ファイザーは、インドでの新型コロナ遺伝子ワクチンの緊急使用の許可申請を取り消したというニュースがありました(『『EXCLUSIVE-Pfizer withdraws application for emergency use of its COVID-19 vaccine in India』REUTER, FEBRUARY 5, 2021』)。
これは、インドではすでにアストラゼネカ製でいくと決まっていたからですが。。。。
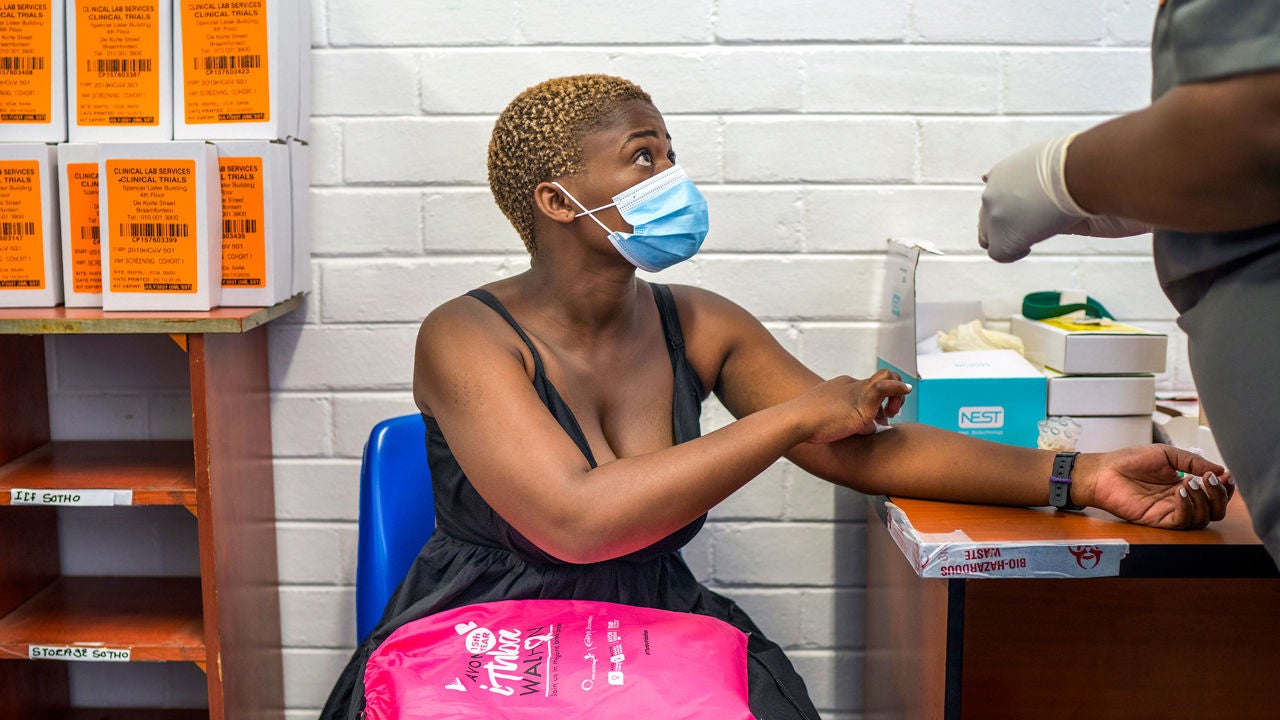
しかし、南アフリカでは、“リアルサイエンス”にもとづいて施行予定のアストラゼネカ製の新型コロナ遺伝子ワクチンの緊急使用の許可を延期したことが報じられています
(『South Africa suspends use of AstraZeneca’s COVID-19 vaccine after it fails to clearly stop virus variant』 Science Mag. Feb. 8, 2021)(『South Africa suspends Oxford-AstraZeneca vaccine rollout after researchers report ‘minimal’ protection against coronavirus variant』 The Washington Post, Feb. 8, 2021)。
その理由は明確です。
2020年に南アフリカでは、アストラゼネカ製の新型コロナ遺伝子ワクチンの臨床試験(フェーズ2/3)に2,000人が参加しています(Lancet. 2020 Dec 8 doi: 10.1016/S0140-6736(20)32661-1)。
アストラゼネカ製の新型コロナ遺伝子ワクチンの臨床試験(フェーズ2/3)は、3カ国の4箇所で行われましたが、なぜか南アフリカだけは、プラセボにきちんと生理食塩水のグループを置いた実験デザインでした。
しかし、この南アフリカの臨床試験の結果だけは、公表されることがなかったばかりでなく、ワクチンの効果や安全性の解析からも除外されたのです(次作参照)。
しかし、今回南アフリカ当局の発表によると、アストラゼネカ製の新型コロナ遺伝子ワクチンは、いわゆる現在流行している変異型(B.1.351)に対して軽度〜中等度の症状の改善さえ、プラセボと変わらないことが判明しています(ワクチン接種したもの 19人およびプラセボ20人が軽〜中程度の症状を発症)。このデータは論文発表される予定のようです。
ワクチンの緊急使用の効果がWHOの推奨基準の50%を下回っていたことが理由で、緊急使用を延期したのです。
もちろん、この臨床試験でもワクチンの真の効果の指標である重症例や死亡などの改善率などは調べるデザインになっていません。
南アフリカの臨床試験参加者は、平均年齢31歳の若くて健康な人たちでした。これは過去のワクチンの実験でも認められるバイアス実験です(healthy user bias)。実際の社会では、むしろ高齢者などの余力がない人に優先的に接種しますから、若くて健康な人を中心とした臨床実験に信頼性がないということです。
すでに南アフリカには、100万回分のアストラゼネカ製の新型コロナ遺伝子ワクチンが届いていて、当局が接種したがっていたようですが、やむなくストップをかけたようです。
日本の厚生省は、これと同じ状況になったときに、同じ判断ができるでしょうか?
日本は“ファクターX”などではなく、ある理由で新型コロナをはじめとしたウイルス感染症からは守られている国です(その他にも守られている国、地域がある)。したがって、本来は、ワクチンなどを必要としない国です。
しかも、現在は緊急使用するような状況にはありません。緊急使用の許可は延期すべきです。購入代金はすでに支払っているので、その点では文句はないはずです(^_−)−☆。