『腸内環境とアルツハイマー病の驚くべき関係:腸内細菌を増やしてはいけない決定的理由』
アルツハイマー病の原因は腸にあった?画期的な研究が明らかにする意外な関連性
最新の研究が、アルツハイマー病と腸内環境の間に驚くべき関連性を発見しました。この画期的な発見は、私たちの日常の食生活がいかに脳の健康に直接影響するかを示しています。
腸から脳へ:見えない敵の正体
研究者たちは、アルツハイマー病患者の脳内に「リポ多糖(LPS)」と呼ばれる強力な神経毒素(内毒素)が異常に多く存在することを発見しました。この毒素は腸内に生息する細菌(グラム陰性桿菌)から生み出されています。
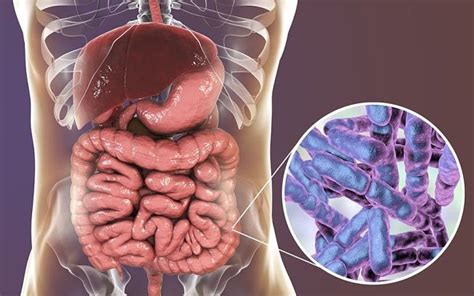
「リポ多糖(LPS)は、私たちが知る最も強力な微生物由来の炎症性神経毒素の一つです」と研究者は説明しています。「世界中の研究チームが、アルツハイマー病患者の脳内でさまざまなリポ多糖(LPS)変異体を確認してきました」
驚くべき侵入経路
この研究で特にLPSは腸のバリアを通り抜け、血液に入り、血液脳関門を突破して、脳のさまざまな部位に到達します。そして、慢性的な炎症を引き起こし、神経の機能を破壊していくのです。
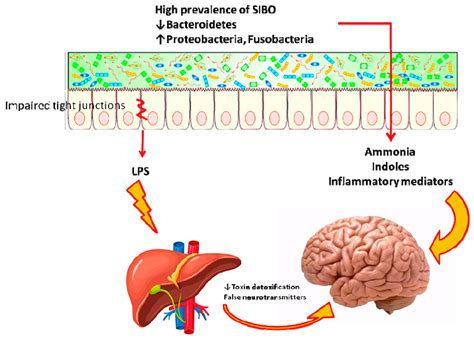
脳内に侵入したLPSは神経細胞に炎症を引き起こし、細胞の構造を保つ重要なタンパク質「神経フィラメント軽鎖(NF-L)」を破壊します。これが神経細胞の萎縮を招き、最終的には細胞死へと導く—アルツハイマー病の特徴的な症状です。
腸内細菌を増やさないことが脳を守る
腸内細菌が大腸で過剰増殖すると、本来は無菌状態の小腸まで細菌が増殖(SIBO)して栄養吸収障害やリポ多糖(LPS)吸収による強い全身の炎症を引き起こします。
今回の研究は同時に大きな希望ももたらしています。日常の食生活での簡単な変化が、この危険なプロセスを防ぐ可能性があるのです。
腸内細菌の餌(エサ)とならない食物繊維を十分に摂取することで、腸内細菌の増殖を抑えて、有害な神経毒素(LPS)の放出を効果的に抑制できます。
実際に「不溶性食物繊維」とよばれる腸内細菌の増殖を抑える栄養素は、LPSの生成を抑え、腸からの吸収を減らすことがわかっています(拙著『慢性病は現代食から』のエビデンス参照)。
特に長年お伝えしてきた生ニンジンのような腸内細菌の増殖を抑える不溶性食物繊維の豊富な食品は、ようやくソーシャルメディアでも話題になってきましたが、アルツハイマー病だけでなく、パーキンソン病や筋萎縮性側索硬化症(ALS)などの神経変性疾患の予防に役立つ可能性があります。

以前マダガスカルのサルが、雷が落ちて燃えた木の炭を食べる行動が観察されていることをお伝えしました。研究では触れられていませんが、活性炭なども腸内細菌の増殖を抑える効果を持ちます。1か月に1回くらいは、腸内を掃除すると脳にも良い影響が出るでしょう。
参考文献
・Downregulation of Neurofilament Light Chain Expression in Human Neuronal-Glial Cell Co-Cultures by a Microbiome-Derived Lipopolysaccharide-Induced miRNA-30b-5p. Front Neurol. 2022 Jun 24:13:900048.
・Facilitation of Gastrointestinal (GI) Tract Microbiome-Derived Lipopolysaccharide (LPS) Entry Into Human Neurons by Amyloid Beta-42 (Aβ42) Peptide.Front Cell Neurosci. 2019 Dec 6;13:545.
・Lipopolysaccharides (LPSs) as Potent Neurotoxic Glycolipids in Alzheimer’s Disease (AD).Int J Mol Sci. 2022 Oct 21;23(20):12671.
・Correlation between the gut microbiome and neurodegenerative diseases: a review of metagenomics evidence.. Neural Regen Res. 2024 Apr;19(4):833-845.
・Lipopolysaccharide-stimulated, NF-kB-, miRNA-146a- and miRNA-155-mediated molecular-genetic communication between the human gastrointestinal tract microbiome and the brain. Folia Neuropathol. 2019;57(3):211-219.