糖質制限(低炭水化物食)では、高脂肪食か高タンパク質食のいずれかにならざるを得ません。
高脂肪食、いわゆるケトン食の害悪は拙著『メタボリック・スイッチ』『慢性病は現代食から』や過去記事等で繰り返しお伝えしてきました。

それでは、高タンパク質食はどうなのでしょうか?

米国式パレオダイエットも高タンパク質食を勧めています。

1回の食事で20gを超える量の高タンパク質を摂取すると、タンパク質の同化(体の構成材料となること)の限度を超えます(How much protein can the body use in a single meal for muscle-building? Implications for daily protein distribution. Journal of the International Society of Sports Nutrition (2018) 15:10)。
タンパク質や糖や脂肪のようにストックがききません。
余剰のタンパク質は私たちの体内でどうなるのでしょうか?

プーファの場合は、ほとんどが燃焼されるか、飽和脂肪酸やコレステロール合成へ使用されます。
過剰のプーファは、脂肪組織だけでなく、各臓器の細胞に入っていきます。
タンパク質も余剰になると分解されてエネルギーとして使用されるようになります(タンパク質への[メタボリック・スイッチ])。
しかし、ここにはプーファ同様、大きな問題が起こります。
タンパク質の分解の過程では、アンモニアが不可避に発生するのです。
アンモニアは、糖のエネルギー代謝をブロックする毒性物質です(Ammonia inhibits energy metabolism in astrocytes in a rapid and glutamate dehydrogenase 2-dependent manner. Dis Model Mech. 2020 Nov 4;13(10):dmm047134)(Effects of acute hyperammonemia in vivo on oxidative metabolism in nonsynaptic rat brain mitochondria. Metab Brain Dis. 1997 Mar;12(1):69-82)(Activities of pyruvate dehydrogenase, enzymes of citric acid cycle, and aminotransferases in the subcellular fractions of cerebral cortex in normal and hyperammonemic rats.Neurochem Res. 1989 Mar;14(3):221-8)(Ammonia mediates mitochondrial uncoupling and promotes glycolysis via HIF-1 activation in human breast cancer MDA-MB-231 cells. Biochem Biophys Res Commun. 2019 Oct 29;519(1):153-159)。
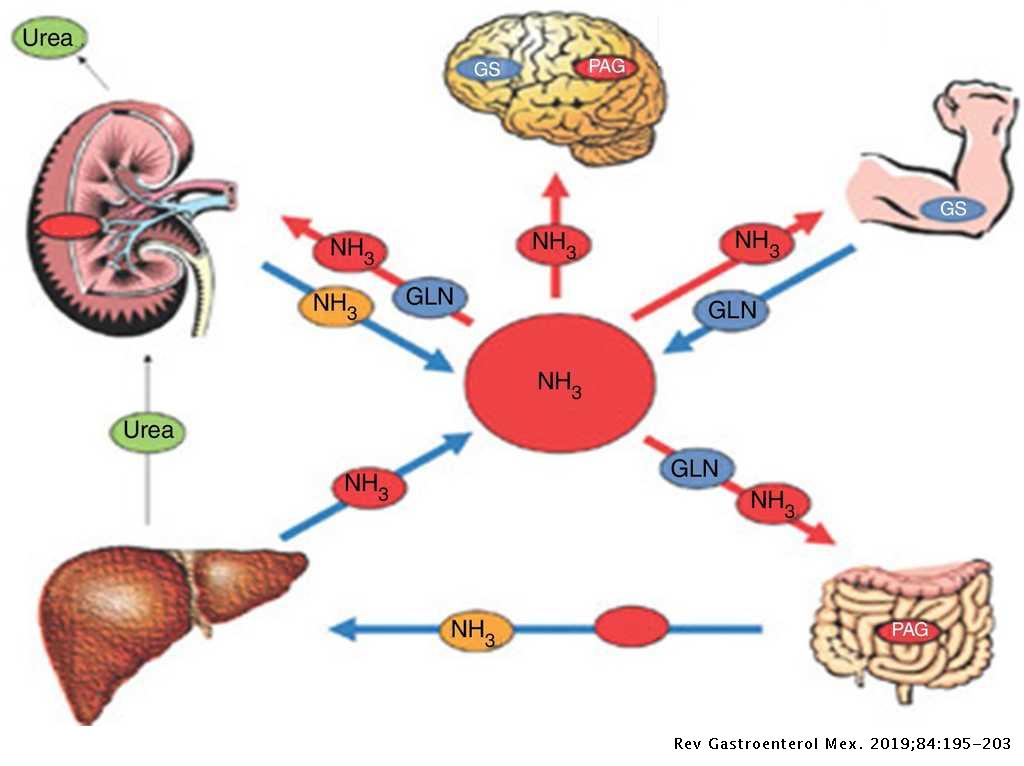
現代医学でさえもアンモニアの神経毒性は認知しているところです。
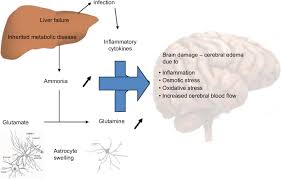
毒性物質のアンモニアは肝臓でデトックスされます。
しかし、このデトックスにはエネルギーと二酸化炭素を要します。

エネルギー(ATP)と二酸化炭素を豊富に供給できるのは、糖のエネルギー代謝が回っていることが必須条件になります。
高齢者に限らず、糖のエネルギー代謝が低下している現代人では、過剰のタンパク質摂取は、アンモニアが蓄積することになるのです。
これに関連して、タンパク質を過剰摂取すると低血糖が起こります(基礎医学参照)。糖質制限では、元々糖質が欠乏しているので、高タンパク質でさらに低血糖に拍車がかかります。

低血糖では、慢性病の原因である「メタボリック・スイッチ」が起こります。

以上から、過剰のタンパク質摂取も目的外に使用されることになるため、病気の場(シックネス・フィールド)を作る原因となります。

糖質制限なる極端な食事法は、 冒頭でお伝えしたように、高タンパク質か高脂肪食になります。
このいずれもが病気の場を作る原因となるのです(^_−)−☆。